Презентация - "Презентация на тему:Химический состав клетки"

- Презентации / Другие презентации
- 0
- 17.03.23
Просмотреть и скачать презентацию на тему "Презентация на тему:Химический состав клетки"
Сайт klass-uchebnik.com предлагает качественные учебные материалы для школьников, родителей и учителей. Здесь можно бесплатно читать и скачивать современные учебники, рабочие тетради, а также наглядные презентации по всем предметам школьной программы. Материалы распределены по классам и темам, что делает поиск максимально удобным. Каждое пособие отличается логичной структурой, доступной подачей материала и соответствует действующим образовательным стандартам. Благодаря простому языку, наглядным схемам и практическим заданиям, обучение становится легче и эффективнее. Учебники подойдут как для ежедневной подготовки к урокам, так и для систематического повторения перед экзаменами.
Особое внимание стоит уделить разделу с презентациями - они становятся отличным визуальным дополнением к теории, помогают лучше понять сложные темы и удерживают внимание учащихся. Такие материалы удобно использовать в классе на интерактивной доске или при самостоятельной подготовке дома. Все размещённые на платформе материалы проверены на актуальность и соответствие учебной программе. Это делает сайт надёжным помощником в образовательном процессе для всех участников: школьников, учителей и родителей. Особенно удобно, что всё доступно онлайн без регистрации и в свободном доступе.
Если вы ищете надежный источник для подготовки к урокам, контрольным и экзаменам - klass-uchebnik.com станет отличным выбором. Здесь вы найдёте всё необходимое, включая "Презентация на тему:Химический состав клетки", чтобы сделать обучение более организованным, интересным и результативным.
Вода.
Количество ее составляет от 60 до 95% общей массы клетки.
Роль воды в клетке определяется ее уникальными химическими и физическими свойствами, связанными главным образом с малыми размерами и полярностью молекул, с их способностью образовывать друг с другом водородные связи.
В зависимости от таксономической и тканевой принадлежности клеток содержание воды может изменяться в широких пределах. Например, в клетках человека среднее содержание воды составляет 40%, в т. ч., в клетках тканей зубов – 3...10%, в клетках жировой ткани – 30...40%, в клетках печени – 75%, в клетках головного мозга 80...85%. В растительных клетках содержание воды достигает 95% за счет клеточного сока.
Роль воды.
Вода—универсальный растворитель для полярных веществ, например солей, сахаров, спиртов, кислот . Вещества, хорошо растворимые в воде, называются гидрофильными. Ее молекулы участвуют во многих химических реакциях, например при образовании или гидролизе полимеров. В процессе фотосинтеза вода является донором электронов, источником ионов водорода и свободного кислорода.
Вода обладает высокой удельной теплоемкостью. Для разрыва водородных связей, удерживающих молекулы воды, требуется поглотить большое количество энергии. Это свойство обеспечивает поддержание теплового баланса организма при значительных перепадах температуры в окружающей среде. Вода отличается высокой теплопроводностью, что позволяет организму поддерживать одинаковую температуру во всем его объеме.
Вода характеризуется высокой теплотой парообразования, т. е. способностью молекул уносить с собой значительное количество тепла при одновременном охлаждении организма. Благодаря этому свойству, проявляющемуся при потоотделении у млекопитающих, тепловой одышке у крокодилов и других животных, транспирации у растений, предотвращается их перегрев.
Для воды характерно исключительно высокое поверхностное натяжение. Это свойство имеет значение для адсорбционных процессов, для передвижения растворов по тканям (кровообращение, восходящий и нисходящий токи в растениях). Многим мелким организмам поверхностное натяжение позволяет удерживаться на воде или скользить по ее поверхности.
Вода обеспечивает передвижение веществ в клетке и организме, поглощение веществ и выведение продуктов метаболизма.
У растений вода определяет тургор клеток, а у некоторых животных выполняет опорные функции, являясь гидростатическим скелетом (круглые и кольчатые черви, иглокожие).
Вода — составная часть смазывающих жидкостей (синовиальной — в суставах позвоночных, плевральной — в плевральной полости, перикардиальной — в околосердечной сумке) и слизей (облегчают передвижение веществ по кишечнику, создают влажную среду на слизистых оболочках дыхательных путей). Она входит в состав слюны, желчи, слез, спермы.
Биологические функции воды в клетках:
1. Служит универсальным растворителем, а также средой для транспорта веществ.
2. Служит средой для протекания химических реакций и сама участвует в них.
3. Обеспечивает относительное постоянство температуры внутри клетки.
4. Служит донором протонов и электронов в обменных процессах.
5Выполняет функцию гидростатического скелета клетки.
6. служит средой для передвижения отдельных клеток.
Неорганические вещества.
Неорганические вещества в клетке, кроме воды, представлены минеральными солями. Молекулы солей в водном растворе распадаются на катионы и анионы. Наибольшее значение имеют катионы К+, Na+, Са2+, Mg2+, NH4+ и анионы (Сl- , Н2Р04 -, НР042- , НС03 -, NO3-, SO4 2- ) Существенным является не только содержание, но и соотношение ионов в клетке.
В составе клеток обнаруживается более половины элементов Периодической системы Д. И. Менделеева. Обязательными является лишь 20: водород, кислород, углерод, азот, фосфор, калий, натрий, кальций, магний, железо, сера, хлор, йод, марганец, кобальт, медь, цинк, молибден, бор, фтор. В очень малых количествах встречаются кремний, селен, хром, стронций и некоторые другие.
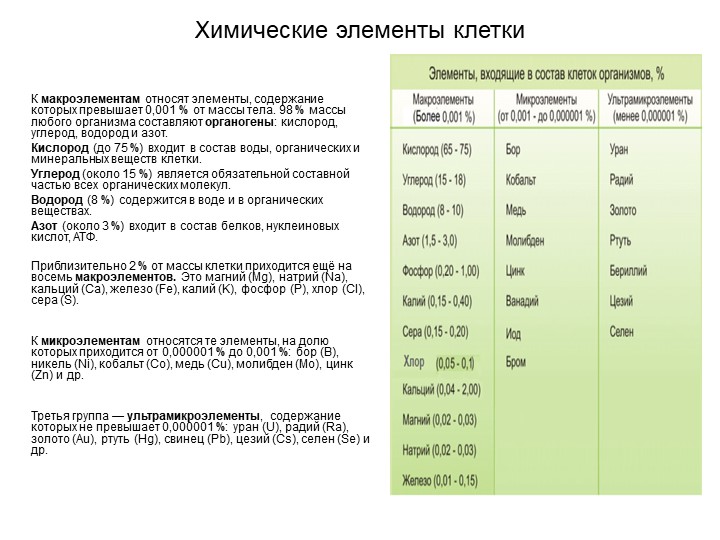
По содержанию в клетке выделяют четыре группы элементов
биогены,
макроэлементы,
микроэлементы,
ультрамикроэлементы.
Биогены.
Элементы, которые обязательно входят в состав биополимеров: кислород (составляет 65...75 % сухого вещества клетки), углерод (15...20 %), водород (8...10 %), азот (1...5 %), фосфор (0,2...1,0%). По массе составляют 98% всего содержимого клетки.
Неорганический кислород.
Представлен молекулярным кислородом О2, входит в состав оксидов и сложных ионов. Эффективным переносчиком молекулярного кислорода в организме высших животных является гемоглобин и сходные с ним вещества (миоглобин, гемоцианин).
Неорганический углерод.
Представлен углекислым газом, который растворен в воде. В водных растворах за счет образования и диссоциации угольной кислоты существует равновесие:
Н2О + СО2 ↔ Н2СО3 ↔ Н+ + НСО3– ↔ 2 Н+ + СО32–
Благодаря действию принципа Ле-Шателье, это равновесие обеспечивает буферность растворов, и в межклеточной среде поддерживается постоянная кислотность (рН).
Неорганический водород.
В клетках представлен протонами, связанными с водой и разнообразными переносчиками. Молекулярный водород встречается только в клетках некоторых бактерий. Атомарный водород в свободном виде в клетках не существует.
Азот.
Поглощается в виде нитрат–ионов и ионов аммония. В органической форме является обязательным компонентом аминокислот, белков и других пептидов, азотистых оснований, нуклеотидов, нуклеиновых кислот и других веществ (хитин, муреин, органические амины).
В неорганической форме представлен нитратами, нитритами и ионами аммония. Аммиак и его производные токсичны для большинства клеток и подлежат удалению.
Нитриты как продукты промежуточных реакций активно взаимодействуют с азотистыми основаниями, изменяя их структуру, то есть являются мутагенами.
Фосфор.
Поглощается в виде кислотных остатков ортофосфорной кислоты Н3РО4: гидрофосфат– и дигидрофосфат–ионов. Остатки ортофосфорной кислоты обозначаются символом Фнеорг. или Ф.
Фосфор в клетке представлен свободными и связанными фосфатами, гидрофосфатами и дигидрофосфатами в составе неорганических и органических соединений.
Фосфаты образуют соединения с макроэргическими связями: АТФ, ГТФ, креатинфосфат, фосфорные эфиры углеводов, жирных кислот.
Фосфаты – обязательный компонент нуклеотидов и нуклеиновых кислот, фосфолипидов.
Макроэлементы.
К макроэлементам относятся элементы, содержание которых в клетках измеряется десятыми и сотыми долями процента сухого вещества клетки (редко содержание достигает нескольких процентов): калий, натрий, кальций, магний, железо, сера, хлор, йод. Содержание макроэлементов в клетках выражается в процентах от всей массы сухого вещества клетки.
Калий.
До 1 %. Поглощается в виде гидратированных ионов К+, которые хорошо проходят через мембраны. Основные функции :
1. Регулирует углеводный обмен.
2. Регулирует осмотическое давление.
3. Участвует в формировании мембранных потенциалов.
4. Активирует ферменты при фотосинтезе.
5. Радиоактивный изотоп 40К – основной источник внутренней радиоактивности.
Натрий.
До 0,1 %. Поглощается в виде гидратированных ионов Na+, которые плохо проходят через мембраны. Регулирует углеводный обмен, осмотическое давление, участвует в формировании мембранных потенциалов.
Кальций.
До 2 %. В клетке представлен гидратированными ионами Са2+, нерастворимыми солями (например, щавелевой, фосфорной, плавиковой кислот), металлорганическими комплексами.
Регулирует активность многих ферментов (например, кальций–зависимой АТФазы в сократимых комплексах), стабилизирует структуру хромосом.
Пектаты кальция – основа срединных пластинок в тканях растений; фториды и фосфаты кальция – основа костной ткани.
Магний.
До 3 %. В клетках содержится в виде металлорганических комплексов, реже – в виде ионов. Стабилизирует структуру рибосом, регулирует активность ферментов, входит в состав АТФазы, входит в состав молекулы хлорофилла в клетках растений.
Железо.
До 0,1 %. Поглощается в виде двухвалентных ионов Fe2+, реже – металлорганических комплексов Fe3+.
В клетках содержится в составе металлорганических комплексов с переменной степенью окисления, реже – в виде ионов Fe2+. входит в состав гема – металлорганического комплекса, содержащего порфириновое ядро и ион железа с переменной степенью окисления.
Гем – обязательный компонент переносчиков кислорода: гемоглобинов и миоглобина. Гем входит в состав различных оксидоредуктаз.
Сера.
До 1 %. Поглощается в виде сульфатов SO42 –. В клетке содержится в виде свободных сульфат-ионов, в окисленной и восстановленной форме в составе органических соединений.
Входит в состав аминокислот: метионина, цистеина; между этими аминокислотами образуются дисульфидные мостики, поддерживающие третичную структуру белка.
Входит в состав кофактора КоА, обслуживающего цикл Кребса и другие обменные процессы.
Хлор.
До 4 %. Поглощается и содержится в клетке в виде хлоридов Cl–.
Участвует в регуляции осмотического давления.
Йод.
До 0,01 %. Содержится в клетках в виде иодидов J– и металлорганических комплексов.
Входит в состав тироксина – гормона щитовидной железы, регулирующего проницаемость мембран.
Микроэлементы.
Элементы, суммарное содержание которых в клетке обычно не превышает 0,01 %.
Содержатся в клетках в виде гидратированных неорганических ионов и (или) металлорганических комплексов.
Марганец.
Участвует в фотосинтезе.
Входит в состав дегидрогеназ и фосфатаз, в состав ферментов, участвующих в симбиогенной фиксации азота.
Активирует ряд ферментов углеводного и азотного обмена.
Кобальт.
Входит в состав нитратредуктаз (катализирует переход нитратов в нитриты).
Кобальт в повышенных дозах необходим для азотфиксирующих бактерий.
Медь.
Входит в состав оксидаз (переносчиков электронов), оксигеназ (например, цитохромоксидазы – комплекса ферментов, присоединяющих электроны к кислороду), дегидрогеназ (переносчиков водорода).
Участвует в синтезе фосфолипидов, гемоглобина.
Цинк.
Входит в состав различных ферментов: карбоангидразы (Н2СО3 → Н2О + СО2), пептидаз (катализируют расщепление белков), дегидрогеназ (например, алкогольдегидрогеназы, катализирующей окисление спиртов до альдегидов).
Входит в состав гормона поджелудочной железы инсулина, регулирующего углеводный обмен.
Регулирует действие гормонов гипофиза.
Молибден.
У азотфиксирующих микроорганизмов входит в состав нитрогеназы – фермента, катализирующего восстановление атмосферного азота до аммиака.
У других организмов входит в состав нитратредуктазы (фермента, восстанавливающего нитраты) и некоторых дегидрогеназ.
Бор.
Регулирует деление клеток меристемы у растений. При его недостатке наблюдаются нарушения развития: слабое ветвление корня, засыхание верхушек побегов, некрозы.
Участвует в регуляции азотного и углеводного обмена.
Ультрамикроэлементы.
Элементы, содержание которых в клетке составляет миллионные доли процента, называются ультрамикроэлементы. К ним относятся: селен, цезий, алюминий, кадмий, ртуть, мышьяк, свинец, серебро, золото, радий и другие.
Биологические функции ультрамикроэлементов изучены недостаточно. В повышенных концентрациях они являются ферментными ядами. Ядовитые свойства ионов металлов часто обусловлены их необратимым связыванием с белками, при этом происходит денатурация белков.
Белки (протеины, полипептиды).
Линейные гетерополимеры, мономерами которых являются α–аминокислоты, связанные между собой пептидными связями.
α –Аминокислоты –органические вещества, в состав которых входит атом углерода, образующий четыре связи: с водородом, с аминогруппой NH2, с карбоксильной группой СООН и органическим радикалом R. В генетическом коде записано только 20 α–аминокислот, в составе полипептидов эти аминокислоты могут изменяться (например, аминокислота пролин в составе белка коллагена окисляется до гидроксипролина).
В клетках встречается свыше 100 α–аминокислот, которые не входят в состав белков, но принимают важное участие в обмене веществ (например, орнитин).
Различают простые и сложные белки .
Простые белки (собственно протеины) состоят только из последовательностей остатков аминокислот, связанных пептидной связью.
Сложные белки (протеиды) содержат, кроме полипептидных цепей, простетическую группу – прочно связанный с полипептидом небелковый компонент. Большинство белков клетки относится к сложным белкам.
Примеры сложных белков:
гликопротеиды (содержат углеводные остатки),
липопротеиды (комплексы из белков и липидов),
нуклеопротеиды (комплексы из белков и нуклеиновых кислот ),
хромопротеиды (содержат пигменты),
флавопротеиды (содержат группу ФАД),
металлопротеиды (содержат ионы различных металлов).
Структура белковых молекул.
Последовательность аминокислот закодирована в ДНК и называется первичной структурой белка. Большинство полипептидов состоит из 100...150 аминокислотных остатков (сокращенно – а.о.). Однако существуют дипептиды (состоят из двух а.о.), олигопептиды (от трех до нескольких десятков а.о.) и гигантские белки (длиной свыше 300 а.о.).
Вторичная структура белков представлена правозакрученной a-спиралью и складчатыми структурами – b-слоями. a-Спираль характерна для миоглобина, a-кератина, b-складки – для иммуноглобулинов, фиброина шелка.
У многих белков вторичная структура представлена чередованием a-спиралей, b-складок и нерегулярных участков.
Встречается и левая спираль, например, у коллагена.
Вторичная структура белков поддерживается за счет водородных связей, возникающих между группами СО и NH.
Третичная структура (конформация)
Общая форма белковой молекулы в пространстве. По форме различают два типа белков: глобулярные (в виде шара) и фибриллярные (в виде нити).
Третичная структура поддерживается за счет гидрофобных и бисульфидных связей между аминокислотными радикалами.
Разрушение третичной структуры белка называется денатурацией. Денатурация может быть вызвана высокой температурой, воздействием ионов тяжелых металлов и другими химическими веществами. Денатурированный белок полностью теряет свои специфические свойства. Существует обратимая и необратимая денатурация.
Четвертичная структура.
Белковые комплексы из нескольких полипептидов.
В большом числе случаев для функционирования белков необходимо объединение нескольких полипептидов (субъединиц) в единый комплекс.
Например, в коллагеновых волокнах три полипептидные цепи закручены в тройную суперспираль.
Функции белков:
1. Ферментативная. Практически все ферменты являются белками.
2. Структурная (коллаген соединительных тканей (у млекопитающих составляет около 25% от общей массы белков), эластин, кератин).
3. Гормональная (инсулин, вазопрессин).
4. Транспортная (например, гемоглобин переносит О2, СО, СО2).
5. Защитная (антитела, фибрин).
6. Сократительная (актин-миозиновый комплекс).
7. Опорная (тубулин микротрубочек).
8. Двигательная. Сократимые и опорные комплексы обеспечивают все виды движения.
9. Гомеостатическая. Практически все белки обладают буферными свойствами, поддерживая постоянную величину рН.
10. Запасающая (овальбумин – запасной альбумин яичного белка).
11. Энергетическая. При гидролизе белков образуются аминокислоты, часть которых окисляется с высвобождением энергии.