Презентация - "Урок на тему "Оксиды серы""

- Презентации / Другие презентации
- 3
- 07.02.23
Просмотреть и скачать презентацию на тему "Урок на тему "Оксиды серы""
Сайт klass-uchebnik.com предлагает качественные учебные материалы для школьников, родителей и учителей. Здесь можно бесплатно читать и скачивать современные учебники, рабочие тетради, а также наглядные презентации по всем предметам школьной программы. Материалы распределены по классам и темам, что делает поиск максимально удобным. Каждое пособие отличается логичной структурой, доступной подачей материала и соответствует действующим образовательным стандартам. Благодаря простому языку, наглядным схемам и практическим заданиям, обучение становится легче и эффективнее. Учебники подойдут как для ежедневной подготовки к урокам, так и для систематического повторения перед экзаменами.
Особое внимание стоит уделить разделу с презентациями - они становятся отличным визуальным дополнением к теории, помогают лучше понять сложные темы и удерживают внимание учащихся. Такие материалы удобно использовать в классе на интерактивной доске или при самостоятельной подготовке дома. Все размещённые на платформе материалы проверены на актуальность и соответствие учебной программе. Это делает сайт надёжным помощником в образовательном процессе для всех участников: школьников, учителей и родителей. Особенно удобно, что всё доступно онлайн без регистрации и в свободном доступе.
Если вы ищете надежный источник для подготовки к урокам, контрольным и экзаменам - klass-uchebnik.com станет отличным выбором. Здесь вы найдёте всё необходимое, включая "Урок на тему "Оксиды серы"", чтобы сделать обучение более организованным, интересным и результативным.
Сера, сера, сера. эс
32-атомный вес.
Сера в воздухе горит-
Получаем ангидрид.
Ангидрид, да плюс вода –
Это будет кислота.
Цели урока:
Изучить физические, химические свойства оксидов серы
рассмотреть экологическую проблему, связанную с оксидами серы
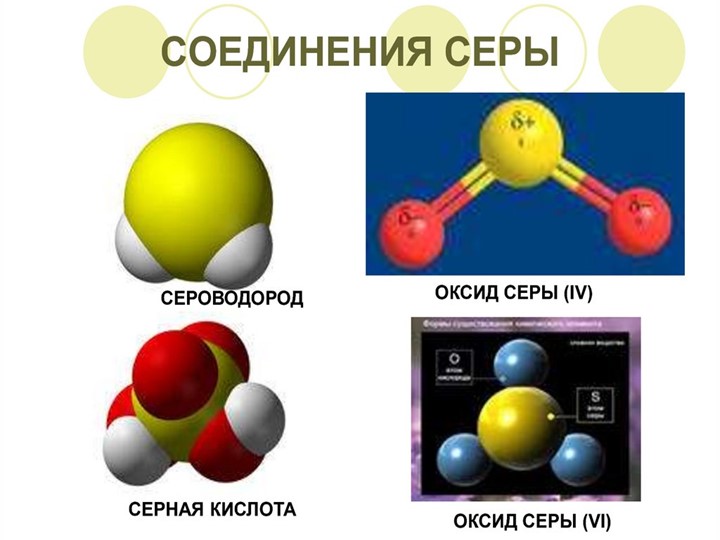
Оксид серы (IV)
Оксид серы (VI)
Сернистый газ
Серный газ
Сернистый ангидрид
Серный ангидрид
2. Физические свойства:___________
2.Физические свойства__________
3. Характер оксида: кислотный
4. Соответствующая кислота: H2SO3
4. Соответствующая кислота: H2SO4
5. Химические свойства с точки зрения кислотно-основных свойств:
А) с водой
Б) с основными оксидами
В) с основаниями
Образование ______________ дождей связано как с _____________ явлениями, так и с ____________________ факторами. Газообразные кислотные оксиды в атмосфере растворяются в парах ______________ и образуют соответствующие ______________. Попадая в почву или водоемы, кислоты ________________ на ионы. Катион ____________ повышает кислотность среды, что является причиной __________ живых организмов. Кислотные дожди несут ___________ для всего живого на планете. Кислотные дожди – реальная _____________ существования человечества.
кислотных
природными
антропогенными
воды
кислоты
диссоциируют
водорода
гибели
опасность
угроза
Из-за нарушения работы вентиляции в помещении лаборатории площадью 25 м2 и высотой потолка 3,2 м в воздухе скопилось 88 мг сернистого газа. Определите и подтвердите расчетами, превышает ли концентрация сернистого газа в воздухе данного помещения значения ПДК. Предложите способ, позволяющий снизить концентрацию сернистого газа в помещении.
Решение:
Найдем объем помещения: V = 25м2 * 3,2 м = 80 м3.
Найдем концентрацию сернистого газа в данном помещении:
C = 88 мг/ 80 м3 = 1,1 мг/м3